Activités page 158 et page 159 : Molécules et atomes
Activité page 158
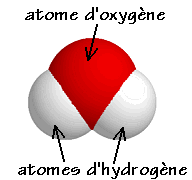
Q1 : La composition d’une molécule d’eau est :
1 atome d’oxygène (O) et 2 atomes d’hydrogène (H).
Sa formule chimique est donc H2O.
Q2:Les symboles chimiques des atomes sont :
Oxygène : O
Azote : N (nitrogen en anglais !)
Carbone : C
| Nom | Représentation | Formule | Composition atomique |
| Dioxygène |
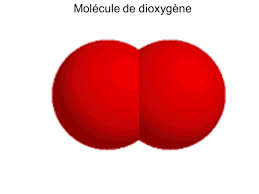 |
O2 | 2 atomes d’oxygène |
| Diazote |
 |
N2 | 2 atomes d’azote |
| Dihydrogène |
 |
H2 | 2 atomes d’hydrogène |
| Dioxyde de carbone |
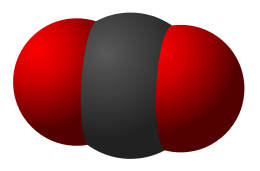 |
CO2 | 1 atome de carbone et 2 atomes d’oxygène |
Q4 : Une molécule est composée d’atomes liés en eux. Nous la représentons en tenant compte de sa composition (type et nombre d’atomes).
Activité p 159 :
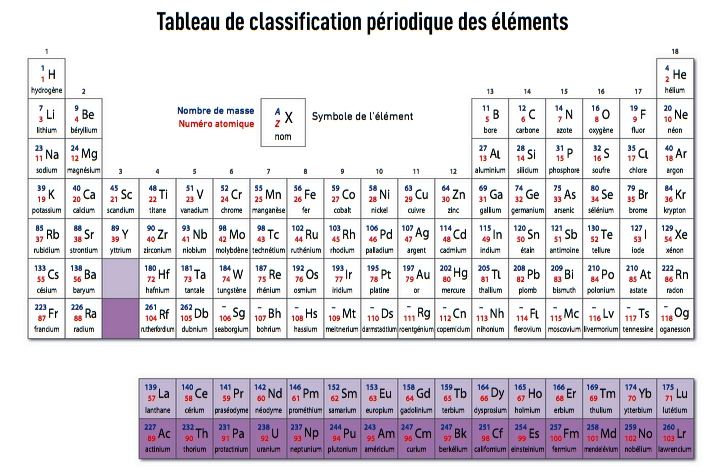
Q1 : Le premier chimiste à avoir classé les atomes est Dimitri Mendeleïv en 1869.
Il laisse des "cases" vides pour les atomes qui, d’après ses hypothèses, restent à découvrir.
Q2:A l’époque, on connaissait 63 types d’atomes. Aujourd’hui, nous en connaissons une centaine.
Un lien vers une classification interactive : ICI
Q3 : Symboles des atomes :
fer : Fe
fluor : F
Q4 : Noms des atomes
C : carbone
Cu : cuivre
Ca : calcium
Q5 : Deux atomes de types différents ne peuvent pas avoir le même symbole chimique. Un symbole chimique ne correspond qu’à un seul type d’atome.
Q6:La grande diversité de molécules s’explique par le nombre quasiment infini de combinaisons que les atomes peuvent former en se liant entre eux !
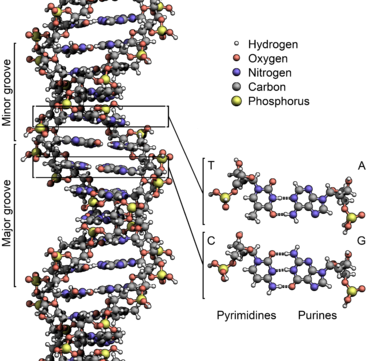
Une macromolécule particulière : l’ADN. Un exemple de la quasi infinité de combinaisons possibles de quelques types d’atomes entre eux !
- Podcast et RSS
- Plan
- Mentions
- Rédaction
- Se connecter

-
2009-2025 © Collège Hubert Fillay - Tous droits réservés
Ce site est géré sous SPIP 3.2.19 et utilise le squelette EVA-Web 4.2

Dernière mise à jour : vendredi 8 avril 2022